قدس آنلاین؛ در سالهای اخیر موفقیتهای کشور در تولید واکسن و واکسیناسیون عمومی به قدری چشمگیر بوده که سازمان بهداشت جهانی ایران را الگویی برای کشورهای منطقه معرفی کرده است؛ این موفقیتها محصول تلاش نخبگان و دانشمندان جوان ایرانی است که در رقابت با دیگر دانشمندان دنیا، باز هم توانستند به رغم تحریمها واکسن کرونا را نیز بومیسازی کنند و در بین ۱۶ کشوری که واکسن کرونا ساختهاند رتبه یازدهم را به خود اختصاص دهند.
ایران واکسیناسیون علیه کووید-۱۹ را با واکسنهای وارداتی اسپوتنیک وی، آسترازنکا/آکسفورد، سینوفارم و کووکسین(بهارات) آغاز کرده است. تا تاریخ ۴ خرداد ،۱۴ تقاضای فعال( در حال انجام) جهت ساخت واکسن کووید-۱۹ به سازمان غذا و داروی کشور ارایه شده است که از بین آنها، ۵ واکسن موفق به اخذ کد اخلاق جهت مرحله بالینی شدند.
اقدام دانشمندان و شرکتهای دارویی و واکسنسازی ایران برای ساخت واکسن کووید-۱۹ اقدام بهجا و مناسبی است. اگر تولید واکسنهای ملی با موفقیت و در موعد مقرر به نتیجه برسد، ایران میتواند زودتر از بسیاری از کشورهای دیگر دنیا پوشش واکسیناسیون خود را کامل کند. بااینحال برای کاهش آسیبهای این بیماری باید کماکان و تا زمان دستیابی به واکسنهای ساخت کشور، ورود واکسن بهسرعت و جدیت دنبال شود. بهخصوص سرعت در انجام واکسیناسیون گروههای در معرض خطر با واکسنهای در دسترس در سریعترین زمان ممکن از آسیبهای این بیماری در کشور میکاهد.
کدام واکسنهای کووید-۱۹ ایران وارد فاز بالینی شدهاند؟
| فاز مطالعه |
نوع واکسن |
| فاز ۳ بزرگسالان |
واکسن مشترک موسسه انستیتو پاستور و موسسه فینلای کوبا (واکسن سوبرانا) |
| فاز ۳ در افراد بالای ۱۸ سال |
واکسن موسسه شفافارمد (واکسن کووبرکت) |
| فاز ۲ بزرگسالان |
واکسن موسسه تحقیقات واکسن و سرمسازی رازی (واکسن کووپارس) |
| فاز ۲ بزرگسالان |
واکسن موسسه میلاد دارو نور (واکسن فخراواک) |
| فاز ۲ بزرگسالان |
واکسن ساخت شرکت تحقیقاتی و تولیدی سیناژن (واکسن سیناژن) |
در ادامه مطالب، ویژگیهای اساسی این پنج واکسن آمده است.
واکسن مشترک موسسه انستیتو پاستور و موسسه فینلای کوبا(واکسن سوبرانا)
انستیتو پاستور ایران از شروع پاندمی کرونا، موضوع تولید واکسن مشترک با کشور کوبا را آغاز کرد. این واکسن حاوی پروتئین نوترکیب از ناحیه RBD ژنوم ویروس Sars-COV-۲ با رژیم ۲ نوبته( با و بدون دوز بوستر)است. که بعد از گذراندن موفق فاز۱ و ۲، وارد فاز سوم کارآزمایی بالینی شده است. مرحله سوم کارآزمایی این واکسن تصادفی شده با گروه پلاسبو و دو سوکور در۲۴ هزار جمعیت ایرانی ۱۸ تا ۸۰ سال در کشور و ۴۴ هزار نفر در کوبا در حال انجام است.
فاز سوم این واکسن در ۷ استان کشور(اصفهان، بابل، زنجان، هرمزگان، مازندران، کرمان، همدان و یزد) بهطور تصادفی در دو گروه در حال اجرا است.
گروه اول: گروه دریافتکننده واکسن(۸۰درصد افراد موردمطالعه)
گروه دوم: گروه پلاسبو یا ادجوانت(۲۰درصد افراد موردمطالعه بهعنوان شاهد)
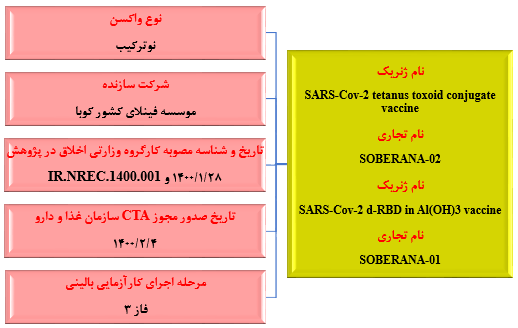
شکل شماره ۲. مشخصات واکسن مشترک موسسه انستیتو پاستور و موسسه فینلای کوبا(واکسن سوبرانا)
واکسن موسسه شفا فارمد (واکسن کووبرکت): فاز ۳ در افراد بالای ۱۸ سال
واکسن کووبرکت نخستین واکسن کووید-۱۹ تولید محققان ایرانی است که موفق به دریافت کد اخلاق و کارآزمایی انسانی از وزارت بهداشت شده است. این واکسن در شرکت شفا فارمد وابسته به بنیاد برکت ستاد اجرایی فرمان امام(ره) تولیدشده است که اکنون در مرحله فاز کارآزمایی قرار دارد. این واکسن از نوع ویروس غیرفعال شده است که کارآزمایی بالینی دو سو کور آن با کنترل پلاسبو فاز ۱ جهت بررسی بیخطری و ایمونوژنیسیتی واکسن در جمعیت سالم و افراد ۵۱ تا ۷۵ ساله انجامشده است.
فاز ۲ و ۳ این واکسن با طراحی کارآزمایی تصادفی، دو سو کور و موازی با گروه کنترل پلاسبو در جمعیت ۱۸ تا ۷۵ ساله در حال انجام است.
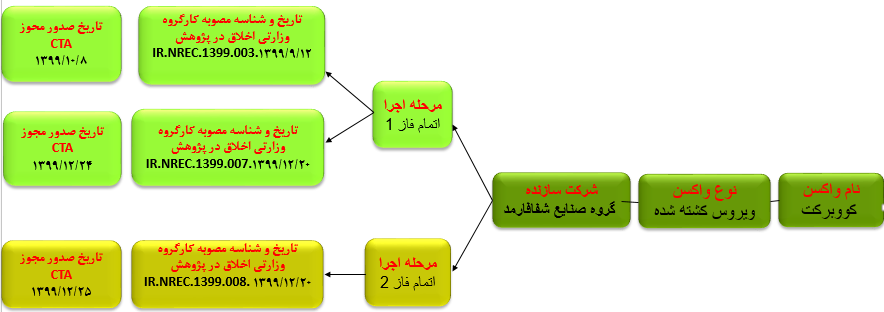
شکل شماره ۳. مشخصات واکسن موسسه شفا فارمد (واکسن کووبرکت)
واکسن موسسه تحقیقات واکسن و سرمسازی رازی(واکسن کووپارس): فاز ۲ بزرگسالان
واکسن کووید-۱۹کووپارس، توسط موسسه تحقیقات واکسن و سرمسازی رازی بر پایه پروتئین نوترکیب اسپایک SARS COV-۲ ساخته و از دو بخش آنتیژن و ادجوانت در سه دوز(تزریقی- استنشاقی، دو دوز اول واکسن بهصورت عضلانی و دوز سوم بهصورت استنشاقی در روز ۵۱ به داوطلبان تزریق میشود) تولید خواهد شد.
شروع واکسیناسیون با واکسن" کووپارس" در ۵۰۰ موش و ۲۵ میمون سبز آفریقایی در مدت یک سال انجام و در ادامه پس از ارسال CTD به سازمان غذا و دارو و دریافت تأییدیههای کمیته اخلاق فاز یک و دو کارآزمایی بالینی ادامه پیدا کرد. فاز یک کارآزمایی بالینی در اسفندماه ۱۳۹۹ آغاز و نیمه فروردینماه با ۱۳۳ جمعیت بزرگسال سالم ۱۸ تا ۵۵ ساله در مطالعهی کارآزمایی بالینی با طراحی موازی، ۴ گروه شامل ادجوانت بهتنهایی و واکسن در دوزهای ۵، ۱۰ و ۲۰ میکروگرم در ۲۰۰ میکرو لیتر به پایان رسید.
فاز دوم کارآزمایی بالینی با حضور ۵۰۰ داوطلب از جمعیت ۱۸ تا ۷۰ ساله در حال انجام است.که در این مطالعه کارآزمایی بالینی با طراحی موازی و دوسوکور، ۲ گروه واکسن و دارونما حضور دارند که انتظار بر این است تا پایان تیرماه ادامه داشته باشد.
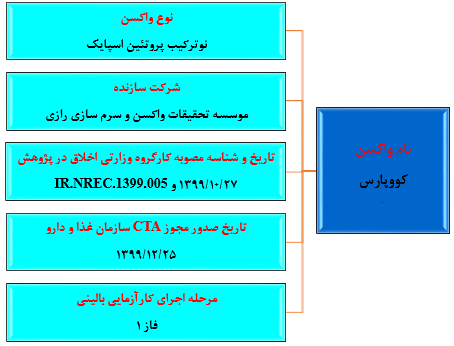
شکل شماره ۴. مشخصات واکسن موسسه تحقیقات واکسن و سرمسازی رازی(واکسن کووپارس)
واکسن موسسه میلاد دارو نور(واکسن فخراواک): فاز ۲ بزرگسالان
واکسن فخراواک "واکسن شهید فخری زاده یا سپند"، واکسنی از نوع ویروس غیرفعال شده است که اسفندماه ۱۳۹۹ موفق به دریافت مصوبه اخلاق در پژوهش از سازمان غذا و دارو شده است؛ واکسنی دو دوزی که تحت مطالعه کارآزمایی بالینی دوسوکور با کنترل پلاسبو موردمطالعه قرار میگیرد. این واکسن محصول شرکت «میلاد دارو نور» در زیرمجموعه وزارت دفاع و پشتیبانی نیروهای مسلح است.
مطالعه فاز یک این واکسن، بررسی بیخطری، ایمنیزایی و انتخاب دوز مناسب واکسن غیرفعال شده کووید-۱۹ (MIVAC) در گروههای واکسن در دو دوز (TCID۵۰) در حال انجام است. این مطالعه در جمعیت سالم بزرگسال ۵۵-۱۸ ساله بهصورت کارآزمایی بالینی تصادفی شده، دوسو کور با کنترل پلاسبو در حال انجام میباشد و فاصلههای دو دوز نیز تقریباً ۲ و ۳ هفته در نظر گرفتهشده است.
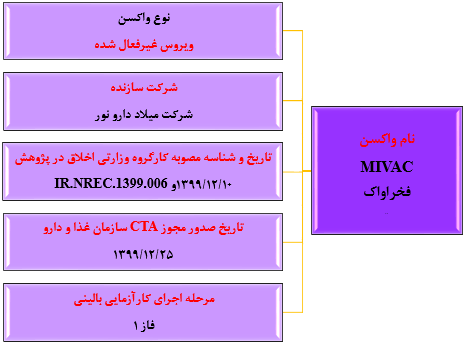
شکل شماره ۵. مشخصات واکسن موسسه میلاد دارو نور(واکسن فخراواک)
واکسن ساخت شرکت تحقیقاتی و تولیدی سیناژن( واکسن سیناژن)
واکسن سیناژن، پنجمین واکسن کووید-۱۹ در ایران است که مجوز کد اخلاق را گرفته است. این واکسن اولین واکسن کرونای ساخت بخش خصوصی در ایران است که به آزمایش بالینی رسیده است و مشترک با کشور استرالیا تولید خواهد شد. درواقع ابتدا توسط یک شرکت استرالیایی به نام "وکسین" که تخصص آن در تحقیقات واکسن است توسعه پیداکرده است و بعد فاز ۱ را با موفقیت بر روی ۴۰ شهروند استرالیایی گذرانده است و اکنون بعد از طی آزمایشات حیوانی و فاز ۱ وارد فاز ۲ خواهد شد. کارآزمایی بالینی فاز دو این واکسن، تصادفی شده، دو سو کور و حاوی واکسن نما جهت بررسی ایمنی و اثربخشی واکسن نوترکیب با پروتئین اسپایک ویروس SARS-COV-۲ (اسپایکوژن) میباشد که در دو دوز ۲۵ میکروگرم به فاصله ۲۱ روز تزریق خواهد شد(مطالعه از اوایل خرداد ما شروع خواهد شد).

شکل شماره ۶. واکسن ساخت شرکت تحقیقاتی و تولیدی سیناژن( واکسن سیناژن)
افق پیش روی واکسنها
خوشبختانه به نظر میرسد ویروس کرونا، واکسن پذیر است. سابقه مطالعات قبلی بر روی سایر ویروسهای این خانواده برای تهیه واکسن و سرمایهگذاریهای کلان توسط کشورها و سازمانهای مختلف بینالمللی به کنترل این باندمی از طریق ساخت واکسن کمک کرد. برآورد میشود تا پایان سال ۲۰۲۱، بین ۸ تا ۲۱ میلیارد دوز واکسن در دنیا تولید شود. افق کشورهای ثروتمند و پیشرفته حصول به ایمنی جمعی با واکسیناسیون قبل از شروع تابستان و یا حداکثر تا ابتدای پاییز است و پیشبینی میشود که تا پایان سال ۲۰۲۱ واکسیناسیون خود را به اتمام برسانند. باید توجه داشت که کشورهایی که فقط به سبد COVAX متکی هستند، نمیتوانند انتظار واکسیناسیون بیش از ۲۰٪ از جمعیت خود را داشته باشند. بنابراین سرمایه گزاری برای تولید و استفاده از واکسنهای داخلی در هر کشوری میتواند یک اولویت مهم و اساسی در مبارزه با این پاندمی باشد.
در صورت موفقیت واکسنهای تولیدی، ایران ضمن دستیابی به تکنولوژی ساخت و کسب دانش برای تولید این واکسن، میتواند با تکیه به واکسنهای تولید داخل کشور زودتر از بعضی از کشورهای دنیا به پوشش لازم واکسیناسیون علیه کووید-۱۹ و احتمال برگشت به زندگی عادی برسد.
اقدام دانشمندان و شرکتهای دارویی و واکسنسازی ایران برای ساخت واکسن کووید-۱۹ اقدام بهجا و مناسبی است. اگر تولید واکسنهای ملی با موفقیت و در موعد مقرر به نتیجه برسد، ایران میتواند زودتر از بسیاری از کشورهای دیگر دنیا پوشش واکسیناسیون خود را کامل کند. بااینحال برای کاهش آسیبهای این بیماری باید کماکان و تا زمان دستیابی به واکسنهای ساخت کشور، ورود واکسن بهسرعت و جدیت دنبال شود. بهخصوص سرعت در انجام واکسیناسیون گروههای در معرض خطر با واکسنهای در دسترس در سریعترین زمان ممکن از آسیبهای این بیماری در کشور میکاهد. پیشنهاد میشود برای جلب اعتماد علمی و عمومی، هرچه سریعتر نتایج مطالعات فاز ۱ و ۲ و در صورت امکان، فاز ۳ مطالعات داخلی چاپ گردد.
انتهای پیام/






























نظر شما